Rappels de seconde

Masse volumique
Solvant, soluté, solution et concentration en masse
Quantité de matière (en mol)
Préparer une solution par dissolution et par dilution
Une équation chimique donne les proportions en quantité de matière selon lesquelles les réactifs réagissent.
On doit donc savoir passer d’une quantité mesurable (masse, volume) à une quantité de matière.
Quantité de matière
Masse molaire
Pour calculer la masse molaire d’une espèce chimique, on ajoute les masses molaires des atomes la constituant.
La masse molaire des atomes est connue et se trouve dans le tableau périodique des éléments.
Question
On donne les masses molaires suivantes (en g/mol) : M(H) = 1,0 ; M(C) = 12,0 ; M(O) = 16,0.
Quelle est la masse molaire moléculaire du méthanol de formule brute CH4O ?
D’une grandeur à l’autre
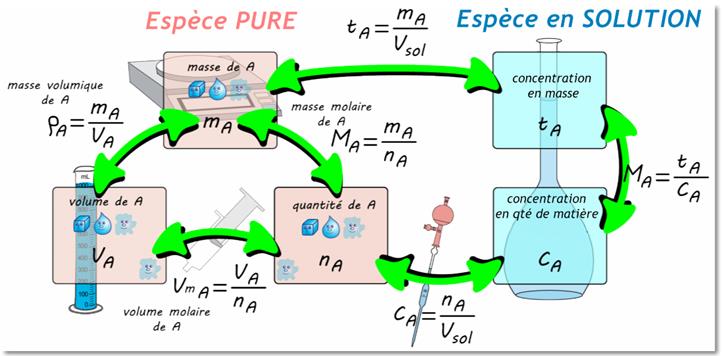
Le schéma ci-dessous résume les différents passages d’une grandeur à l’autre.

Il faudra toujours se demander en premier lieu si on a affaire à un corps pur (en rose) ou un mélange (en bleu) ou si on passe de l’un à l’autre.
Les unités sont un moyen de vérifier (voire retrouver) les formules.
Question
Un carreau de sucre (C6H12O6) de dimensions 2,0 x 1,6 x 1,1 cm et de masse 5,95 g est dissous dans un verre d’eau (20 cL).
Calculer la quantité de matière de sucre dans le morceau et la masse volumique du carreau de sucre.
Dissolution et dilution
La technique
On se reportera à ce qui a été vu en seconde pour ce qui est de la préparation des solution (cliquer sur le lien ci-dessous)
Les concentrations
Selon les besoins on calculera la concentration en masse (vue en seconde) ou la concentration en quantité de matière.
Concentration en masse
\Large \boxed{C_m = \frac{m_{soluté}}{V_{solution}}}

C_m en g.L-1
m en g
V en L
Concentration en quantité de matière
\Large \boxed{C = \frac{n_{soluté}}{V_{solution}}}

C en mol.L-1
n en mol
V en L
Question
Calculer pour le carreau de sucre de 5,95 g dissous dans 20 cL d'eau les concentrations en masse et en quantité de matière de la solution d’eau sucrée obtenue.

